
📋 건강기능식품 GMP 인증 절차부터
실무 운영 전략까지
건강기능식품 GMP는 철저한 품질관리 시스템으로, 확실히 소비자 안전을 보장하고 제품 품질의 일관성을 유지하는 필수적인 품질 인프라입니다.
🔍 건강기능식품 GMP의 개념과 중요성
GMP(Good Manufacturing Practice)는 '우수 제조 및 품질관리기준'입니다.
건강기능식품 산업에서 제품 안전성과 효능을 보장하는 필수 품질관리 시스템입니다.
「건강기능식품에 관한 법률」 제8조, 제14조에 법적 근거가 있으며,
식의약품안전처가 세부 기준을 고시해 운영하는 국가 공인 제도입니다.
건강기능식품 전체 제조 과정에서 일관된 품질과
소비자 안전을 보장하는 체계적인 관리 체계입니다.
📋 건강기능식품 GMP 인증의 필수 요소
건강기능식품은 GMP 적합업소 지정을 받은 제조소에서만
법적으로 생산할 수 있습니다.
이 인증을 받으려면 위생·문서·시험관리·교육 등
품질시스템 전반에 대한 평가를 통과해야 합니다.
단순한 시설 청결이나 기본 위생관리만으로는 부족하며,
문서 기반 품질경영체계가 필요합니다.
이는 원료 입고부터 제품 출하까지 모든 생산 단계를
추적할 수 있는 기록 관리와 검증 절차를 갖춰야 함을 의미합니다.
GMP는 제품 품질의 일관성 유지와 잠재적 위험 예방을 위한 품질관리 체계로,
건강기능식품 산업의 핵심 기반입니다.

🔎 건강기능식품 GMP 인증 프로세스와 법적 체계
건강기능식품 GMP 인증은 명확한 법적 체계와 인증 절차에 따라 진행됩니다.
식약처는 제조업체의 품질 관리 능력을 꼼꼼히 평가합니다.
서류 심사와 현장 실사를 통해 시설 위생, 품질 관리 시스템,
문서화, 직원 교육 등을 점검합니다.
아래 표는 GMP 인증의 핵심 요소와 법적 근거를 요약한 것입니다.
| 항목 | 내용 |
| 관련 법령 | 「건강기능식품에 관한 법률」 제8조, 제14조 등 - 건강기능식품의 제조·품질관리 기준 및 영업자의 준수사항 규정 |
| 운영 주체 | 식품의약품안전처(MFDS) - 인증 심사, 사후관리 및 관련 고시 제·개정 총괄 |
| 인증 대상 | 건강기능식품 제조소(원료 및 완제품 모두 포함) - 국내 유통 목적의 모든 건강기능식품 제조시설 |
| 인증 유효기간 | 3년(정기 실사 및 변경 시 재심사 포함) - 기간 만료 3개월 전 갱신 신청 필요 |
✅ 건강기능식품 GMP 인증 흐름
- 사전 신청 및 자체 점검
- 제조소 관리기준 문서화 및 시설·설비 요건 충족 여부 자체 평가 - 현장 실사 (식약처 또는 지정기관)
- 서류 심사 및 제조시설 현장 점검을 통한 적합성 평가 - 적합 여부 판정 → 'GMP 적합업소' 지정
- 심사 결과에 따른 인증서 발급 및 공식 등록 - 3년 주기 정기 심사 및 변경관리 평가
- 주요 설비·공정 변경 시 변경관리 절차에 따른 재평가 진행

🔖 건강기능식품 GMP 주요 관리 항목 및 실무 요구사항
건강기능식품 GMP는 7가지 핵심 관리 항목으로 구성된 품질관리 시스템입니다.
각 항목은 제품 안전성과 품질 일관성을 보장하기 위한 구체적인 요건을 포함합니다.
제조업체는 모든 요건을 충족해야 '적합업소' 인증을 받을 수 있습니다.
GMP 심사는 항목별 기준에 따라 엄격하게 진행되며,
특히 문서와 실제 운영 일치 여부를 중점 검토합니다.
아래 표는 GMP 관리 체계의 핵심 항목과 주요 요구사항을 정리한 것으로,
인증 준비와 유지 관리에 실용적인 가이드라인을 제공합니다.
근거: 「건강기능식품 제조업체의 제조 및 품질관리기준」 (식약처 고시 제2021-92호)
| 관리 항목 | 주요 요구 사항 |
| 제조소 위생관리 | 작업장 구획화, 출입 통제, 교차오염 방지, 청소 SOP |
| 작업자 위생관리 | 건강검진, 교육훈련, 위생복 착용 및 이력 관리 |
| 자재·원료 관리 | 입고검사, 유효기간 설정, 부적합품 관리, 자재 추적성 확보 |
| 제조공정 관리 | 제조지시서 기반 작업, 공정 간 이탈 방지, 중간점검 체계 |
| 품질시험 관리 | 자체 시험 또는 위탁 시험, 시험 SOP 및 결과 기록 유지 |
| 문서화 시스템 | SOP, 제조기록서, 시험기록서, 변경·이탈 관리 및 개정이력 |
| 자율점검 운영 | 연 1회 이상 실시, 보고서 보관, 개선활동(CAPA) 실행 |
📌 시험은 자체 수행과 공인기관 위탁 모두 인정되며,
명확한 시험관리 책임소재와 체계적인 결과 검토 절차는
반드시 문서화해야 합니다.
⚖ 품질관리 체계 비교: 건강기능식품, 의약품, 일반식품 GMP
건강기능식품 GMP는 다른 산업의 GMP 시스템과 구체적인 차이점이 있습니다.
건강기능식품, 의약품, 일반 식품은 모두 안전성과 품질을 추구하지만,
규제 수준이 다릅니다.
건강기능식품 GMP는 엄격한 의약품 GMP와 기본적인 식품 위생관리 사이에 있는
중간 수준 시스템입니다.
문서화, 시험관리, 변경관리, 자율점검 요구사항에서 뚜렷한 차이가 있습니다.
아래 표는 세 산업 간 GMP 요구사항의 주요 차이점을 정확히 비교해,
각 산업의 품질관리 접근법을 쉽게 이해할 수 있게 합니다.
| 항목 | 건강기능식품 GMP | 제약 GMP | 일반 식품 제조 |
| 법적 구조 | 제조소 단위 인증제 | 품목별 허가 + GMP 적합성 판정 |
위생관리 중심, HACCP 선택적 적용 |
| 심사주기 | 3년마다 정기 심사, 변경 시 재평가 |
GMP 준수 여부 정기 실사 및 보고 의무화 |
위생 점검 위주, 법정 심사 없음 |
| 자율점검 운영 | 연 1회 이상 필수, 보고서 보관 |
연 1회 이상 및 CAPA 보고 의무 |
자율 운영, 법적 요구사항 없음 |
| 시정조치(CAPA) | 권고사항, 수출 시 자발적 운영 필요 |
의무 운영, 교육·조치 이력 필수 |
단순 개선·보완 조치 중심 |
| 문서화 수준 | 제조·시험기록 중심 문서화(SOP 권장) |
전 공정 실시간 기록, 변경관리 필수 |
생산일지 수준, 간소화된 문서화 |
| 시험체계 | 자체 또는 위탁 시험 (책임자 지정 필수) |
전담 QC 조직 운영 필수 | 자가품질검사 또는 위탁 가능(간소화 가능) |
📌 건강기능식품 GMP는 의약품보다는 간소화되어 있으나,
일반 식품과 비교했을 때 확실히 더 엄격한 품질관리 기준과
체계적인 문서 시스템을 요구합니다.
🔑 건강기능식품 GMP 실무 운영의 핵심 포인트
건강기능식품 GMP를 효과적으로 적용하려면
확실한 체계적 접근과 철저한 관리가 필수적입니다.
단순 위생 관리가 아닌 전체 품질 시스템에 대한
명확한 이해와 일관된 실행이 반드시 필요합니다.
제조 현장에서는 철저히 문서화된 절차, 명확한 책임 배분,
지속적 모니터링이 확립되어야 합니다.
이러한 탄탄한 기본 틀 위에 다음과 같은 실무 중심 핵심 전략을 적용하면
효율적이고 안정적인 GMP 시스템을 성공적으로 구축할 수 있습니다.
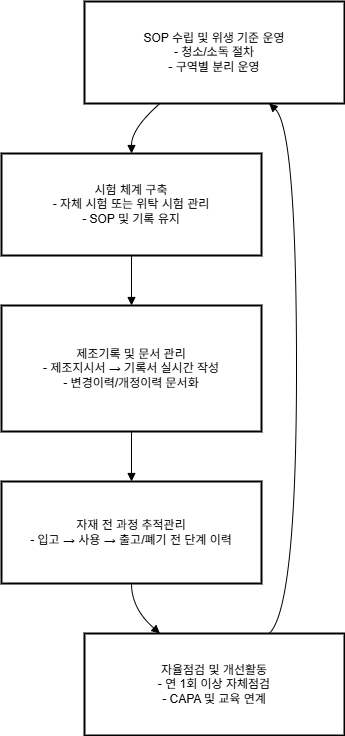
✅ 위생 기준의 구획화 및 SOP 도입
- 원료, 제조, 포장, 완제품 보관 구역의 물리적 분리
- 청소, 소독, 점검 절차의 SOP 기반 운영
✅ 문서화 기반 제조기록 관리
- 제조지시서에서 제조기록서까지 실시간 작성 및 보관
- 변경이력 및 기록 개정 이력의 체계적 문서화
✅ 자재관리 전 과정 추적 체계화
- 입고검사부터 사용처 기록, 출고/폐기까지 전 단계 추적관리
✅ 시험 체계 구축 또는 위탁 관리
- 시험 SOP 수립 및 결과 기록의 체계적 유지
- 위탁 시험의 경우 시험계약서와 관리 SOP 문서화
✅ 자율점검 및 개선활동 연계
- 연 1회 이상의 체계적 자체점검 실시
- 개선사항의 CAPA 기반 보고 및 교육 프로그램 반영
💡 건강기능식품 GMP 체계 주요 정리 및 실천방안
🔎 건강기능식품 GMP 체계의 특성
건강기능식품 GMP는 식약처가 제조소 단위로 인증하는 강력한 품질관리 체계입니다.
위생, 문서, 시험, 자율점검이 체계적으로 통합된 시스템으로
제품 생산 전 과정을 철저히 관리합니다.
이는 단순한 규제 준수를 넘어 제품 안전성과 품질 일관성을
확실히 보장하는 핵심 체계입니다.
📊 건강기능식품 GMP 요구사항 특징
의약품 GMP보다 간소화된 문서 요건이 적용되지만,
일반 식품 제조보다 분명히 더 엄격한 문서 기반 품질 관리가 필요합니다.
이는 국제 시장 진출, 수출 경쟁력 강화, 브랜드 신뢰도 확립,
소비자 안전 보장을 위한 필수적인 인프라로
기업의 지속적 성장에 직접적으로 기여합니다.
🚀 성공적인 건강기능식품 GMP 운영 전략
👉 체계적인 SOP 정비와 주기적 업데이트
👉 정밀한 시험 결과 기록 체계화
👉 철저한 자율점검 실시
👉 효과적인 교육 프로그램 운영
이러한 전략들은 GMP 적합업소 요건을 완벽히 충족하고
지속적인 품질 개선을 이루는 핵심이며,
이를 통해 건강기능식품의 안전성과 효능을 확실히 보장할 수 있습니다.
❓ 건강기능식품 GMP 관련 주요 질문과 답변
Q1. 건강기능식품 GMP는 의약품 GMP만큼 까다로운가요?
→ 건강기능식품 GMP는 의약품 GMP보다 명확히 간소화된 구조를 갖추고 있으나, 일반 식품 제조 기준과 비교하면 확실히 더 엄격한 기준을 적용합니다. 문서화 수준, 자율점검, 시험관리 등에서 분명한 품질 시스템 구축이 요구됩니다. 의약품 수준의 QA 체계에는 미치지 않지만, 식약처 인증을 획득하기 위해서는 위생·문서·시험·교육 전 영역에 걸친 체계적이고 철저한 운영이 반드시 필요합니다.
📌 근거:
- 식약처 고시 「건강기능식품 제조업체의 제조 및 품질관리기준」 제2021-92호
- 식약처 「건강기능식품 GMP 가이드라인」 (2021)
Q2. 자체 시험실이 없어도 건강기능식품 GMP 인증이 가능한가요?
→ 네, 확실히 가능합니다. 건강기능식품 GMP에서는 위탁 시험을 공식적으로 인정하고 있습니다. 다만, 시험 책임자 지정, 시험 SOP 보유, 결과 기록 관리, 위탁계약 문서화 등 시험 품질관리 책임은 여전히 제조업체에게 있으며 이를 철저히 이행해야 합니다. 위탁 시험을 선택하더라도 품질관리 책임은 결코 면제되지 않습니다.
📌 근거:
- 식약처 고시 「건강기능식품 제조업체의 제조 및 품질관리기준」 제6조(시험관리)
- 식약처 「건강기능식품 GMP 운영 가이드」
'GMP 기초 > 산업별 GMP 적용' 카테고리의 다른 글
| 동물용의약품 GMP의 법적 체계와 사람용 GMP와의 차이점 분석 (2) | 2025.05.20 |
|---|---|
| 식품 산업의 GMP와 HACCP 시스템 비교 및 통합 운영 전략 (0) | 2025.05.20 |
| 화장품 GMP와 ISO 22716 기반 품질관리 체계 (0) | 2025.05.19 |
| 의약외품 GMP 적용 기준 및 품질관리 (0) | 2025.05.19 |
| 의료기기 품질관리 시스템:GMP와 ISO 13485 완벽 가이드 (0) | 2025.05.19 |